Sanità
Un solo vaccino contro influenza e Covid. L'Europa approva il primo scudo immunitario combinato al mondo. E' realizzato da Moderna
Via libera della Commissione Ue: le dosi saranno disponibili per gli over 50 in tutti i 27 Stati membri

Il primo vaccino anti Covid di Moderna
Una sola iniezione per proteggersi da due nemici respiratori che ogni inverno mettono a dura prova ospedali e pazienti. La Commissione europea ha concesso l'autorizzazione all'immissione in commercio del primo vaccino combinato anti-influenza e anti-Covid al mondo, sviluppato da Moderna sulla base della tecnologia a mRna. Il via libera - fondato sul parere positivo del Comitato per i medicinali a uso umano dell'Agenzia europea del farmaco Ema - è valido in tutti e 27 gli Stati membri dell'Unione, oltre che in Islanda, Liechtenstein e Norvegia. Il prodotto è destinato agli adulti dai 50 anni in su e diventa il quarto vaccino autorizzato di Moderna nel mercato europeo.
Il via libera non è arrivato per intuizione, ma per dati. Lo studio clinico di fase 3, rsu due gruppi indipendenti di circa quattromila adulti ciascuno, ha valutato sicurezza, tollerabilità e risposta immunitaria del vaccino su due fasce d'età distinte: gli over 65 e gli adulti tra i 50 e i 64 anni. Tutti gli endpoint primari di non inferiorità sono stati raggiunti. Dopo una singola dose, il vaccino combinato ha indotto risposte immunitarie statisticamente superiori contro tre ceppi influenzali (A/H1N1, A/H3N2 e B/Victoria) e contro il Sars-CoV-2 in entrambi i gruppi. L'unica eccezione riguarda il ceppo B/Yamagata, già eliminato dalle raccomandazioni per i vaccini stagionali e quindi non più rilevante sul piano pratico. Il profilo di sicurezza è risultato accettabile, con effetti indesiderati nella maggior parte dei casi solo lievi o moderati, in linea con quanto già noto per i singoli vaccini.
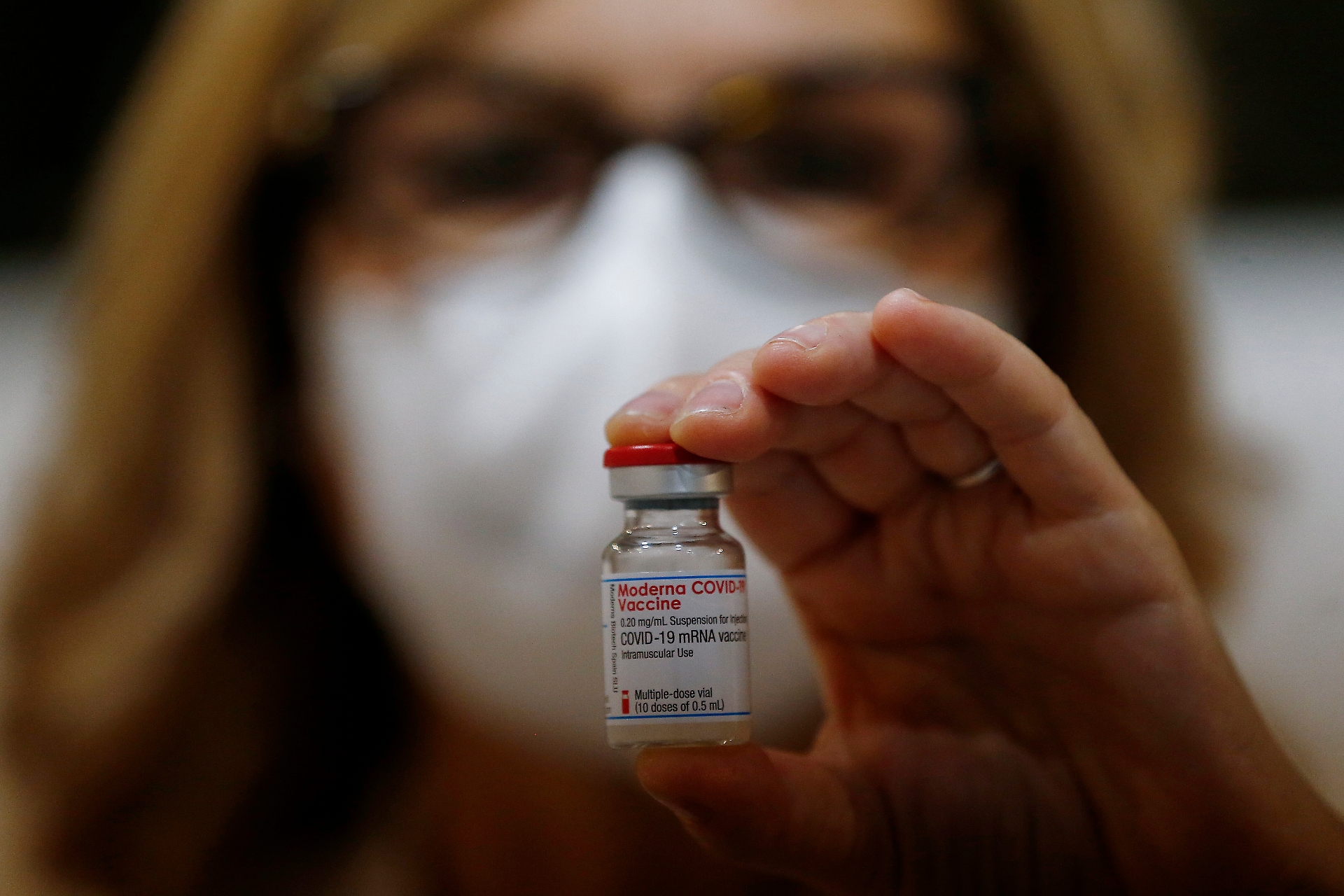 Una sola dose per due virus (foto d'archivio)
Una sola dose per due virus (foto d'archivio)
Ogni anno, la campagna vaccinale autunnale si scontra con un ostacolo silenzioso ma potente: la complessità. Ricordare due appuntamenti, gestire due iniezioni, convincere i più scettici a presentarsi due volte. Un vaccino combinato taglia questo nodo alla radice. "Combinando la protezione contro due importanti virus respiratori in una singola dose, il nostro vaccino mira a semplificare l'immunizzazione per gli adulti, in particolare quelli ad alto rischio", ha dichiarato Stéphane Bancel, Ceo di Moderna. Un beneficio che ricade non solo sui pazienti, ma sull'intero sistema sanitario: meno logistica, meno sprechi, più risorse liberate per altri bisogni. "Questa innovazione introduce un cambio di paradigma nella gestione delle patologie respiratorie", ha sottolineato Cinzia Marano, amministratrice delegata di Moderna Italia, parlando di uno strumento capace di "ottimizzare i percorsi B, ridurre la complessità organizzativa e migliorare l'allocazione delle risorse".
L'autorizzazione europea è il primo passo, ma non l'ultimo. La disponibilità concreta del vaccino in ciascun Paese sarà subordinata alle procedure normative e di accesso nazionali. Moderna ha annunciato che collaborerà con le autorità dei singoli Stati per supportare l'implementazione locale. I tempi, per ora, restano da definire. Quel che è certo è che la strada è aperta. E che la prossima stagione influenzale potrebbe essere la prima in cui milioni di europei over 50 si siedono davanti al medico di base per ricevere, con una sola puntura, la protezione contro due delle minacce respiratorie più diffuse degli ultimi anni.
*Iscrivendoti alla newsletter dichiari di aver letto e accettato le nostre Privacy Policy










